7月7日,廣東省藥品監督管理局在其官網發布消息,決定發布第三批粵港澳大灣區內地臨床急需進口港澳藥品醫療器械目錄。此次公布的目錄中,共引進4種新藥和8種醫療器械。同時將勞拉替尼片移出第一批粵港澳大灣區內地臨床急需進口港澳藥品醫療器械目錄。
公告顯示,此次新引進的4種新藥分別為伊匹木單抗注射液、英克西蘭、依瑞奈尤單抗和巴氯芬注射液。批準進口使用的醫療機構包括香港大學深圳醫院、廣州和睦家醫院和中山陳星海醫院。
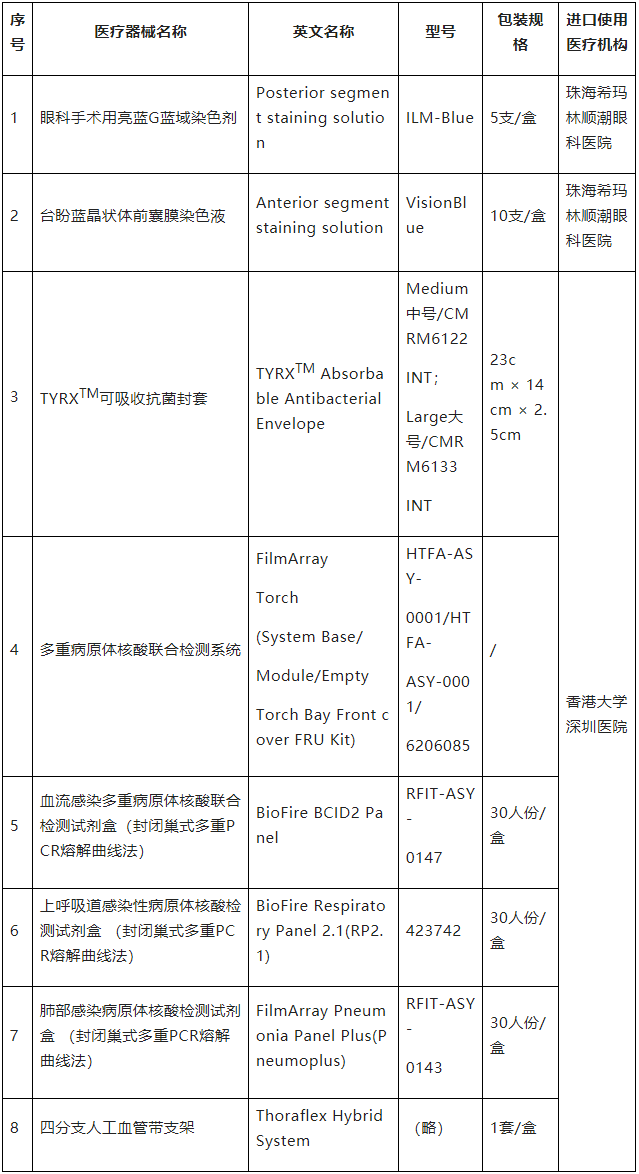
在新增的8種醫療器械中,包括眼科手術用亮藍G藍域染色劑和臺盼藍晶狀體前囊膜染色液2種眼科使用的醫療器械,批準進口使用的醫療機構為珠海希瑪林順潮眼科醫院。另外5種醫院均為香港大學深圳醫院進口使用,分別是TYRXTM可吸收抗菌封套、多重病原體核酸聯合檢測系統、血流感染多重病原體核酸聯合檢測試劑盒、上呼吸道感染性病原體核酸檢測試劑盒以及肺部感染病原體核酸檢測試劑盒。
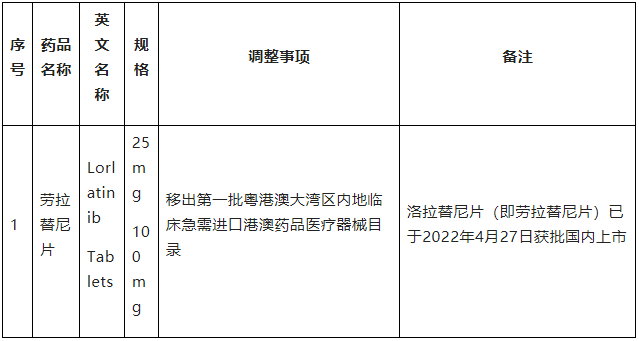
此外,由于洛拉替尼片(即勞拉替尼片)已于2022年4月27日獲批國內上市,本次公告還將勞拉替尼片移出了第一批粵港澳大灣區內地臨床急需進口港澳藥品醫療器械目錄。
延伸閱讀
廣東省藥品監督管理局 廣東省衛生健康委員會
關于發布第三批粵港澳大灣區內地臨床急需進口港澳藥品醫療器械目錄的通告
根據《粵港澳大灣區藥品醫療器械監管創新發展工作方案》(國市監藥〔2020〕159號)和《廣東省粵港澳大灣區內地臨床急需進口港澳藥品醫療器械管理暫行規定》(粵藥監規許〔2021〕4號)要求,結合工作實際,廣東省藥品監督管理局、廣東省衛生健康委員會決定發布第三批粵港澳大灣區內地臨床急需進口港澳藥品醫療器械目錄。通告如下:
一、藥品目錄
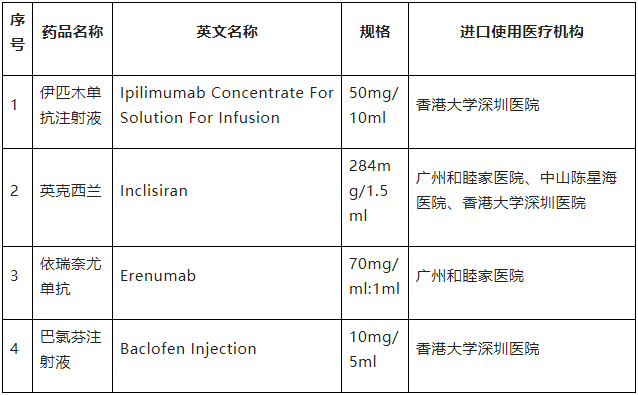
注:伊匹木單抗注射液適應癥為“適用于不可切除或轉移的惡性黑色素瘤、中/高危晚期腎細胞癌以及表皮生長因子受體(EGFR)基因突變陰性或間變性淋巴瘤激酶(ALK)陰性的轉移性非小細胞肺癌”。
二、醫療器械目錄
三、已批準目錄調整
特此通告。
廣東省藥品監督管理局 廣東省衛生健康委員會
2022年7月1日
(記者 何梓陽)
掃一掃,分享到微信朋友圈